Объем газа в 50 литровом баллоне
Re: А сколько кубов газа в 50л баллоне?Я правильно > считаю, что примерно 10?
> В баллоне 42л сжиженного газа.
В бытовом баллоне 50 литров получается 10 куб газа, проверено экпериментально (стоит счетчик). При условии заправки пустого баллона 40-41 литров газа.
Здравствуйте. Сколько литров газа содержится в в 50-литровом баллоне? На сколько его хватает?
Для того, чтобы оставить свой ответ на вопрос
Необходимо авторизоваться Или пройти быструю процедуру регистрации
Зарегистрироваться!
Технические газы – это специальные вещества, получаемые из атмосферы путём разделения, а также из углеводородного сырья во время определенных химических реакций. В большинстве случаев технические газы используются в промышленных, а также бытовых целях, в том числе во время строительства и сварки. Количество содержимого баллонов, измеряют как в килограммах, так и в литрах.
Современная промышленность предполагает образование смесей, которые включают в себя несколько компонентов – газов.
Вне зависимости от вида технического газа или газовой смеси, предполагается её хранение и транспортировка в специальных баллонах. В частном пользовании довольно популярны баллоны на 50 литров.
Рассмотрим сколько литров газа в 50 литровом баллоне содержится по факту? Ответы на поставленный вопрос могут быть разными, так как они зависят от молекулярной массы вещества и степени сжатия газа.
- Углекислота – 24, 6 килограммов.
- Пропан – 21 килограмм или 40 литров.
- Азот и аргон – 10 – 12 килограммов.
- Гелий – 8 – 10 килограммов.
- Ацетилен – 6 килограммов.
50-литрового баллона с пропаном для отопления большого дома, в лютую зиму, хватит на сутки, в остальных случаях – максимум на неделю. Баллон с газом для приготовления еды может использоваться, как минимум, месяц.
Баллонов с газом при сварке потребуется много, ориентировочно – 10 литров – 300 минут, 40 литров – 1200 минут.
Принимая во внимание подобные значения, можно понять, что 50-литровый баллон с газом – это не слишком значительные запасы.
Сколько газа помещается в 50-литровый баллон? Ни для кого не секрет, что объем измеряется в литрах. Многие еще со школьной скамьи помнят о том, что у разных веществ, разная плотность, поэтому и их вес, несмотря на одинаковый объем, может отличаться. Часто твердые вещества, обычно тяжелее, чем жидкости. Однако самый легкий вес у газообразных веществ. Поэтому их иногда закачивают в сжиженном виде (сжижают), чтобы поместилось больше. Так как многие приобретают газ для использования в бытовых целях, в качестве топлива для авто и т. д., их интересует, сколько литров газа в 50 литровом баллоне, или в других объемах. Но, 50 литров – это стандарт, поэтому чаще всего интересуются именно тем, сколько газа в таком баллоне.
Дать точный ответ на данный вопрос достаточно сложно, если учесть, что редко используется чистый газ. Если допустить, что в баллоне чистый пропан, объем будет равен 22,44 м3, если бутан – 16,67 м3. Тем не менее, нередко используется смесь этих газов, поэтому в среднем в 50-литровый баллон помещается около 20 кубометров.
Вопрос «Сколько литров газа в 50-литровом баллоне» вводит некоторых людей в ступор – баллон на 50 литров должен вмещать эти же 50 литров сжиженного газа. Но баллон – хранилище газа, находящееся под давлением. Газ (пропан-бутан) в баллоне находится сразу в двух состояниях – большую часть баллона занимает пропан в жидком состоянии, еще некоторая часть газа существует внутри баллона как раз в газообразной форме.
При изменении температуры газ в баллоне изменяет свой объем, при повышении температуры происходит расширение пропан-бутана и увеличение давления газа на стенки баллона изнутри. Таким образом, ответ на вопрос, сколько литров газа помещается в 50-литровом баллоне, неочевиден.
Как перевести килограммы пропан-бутана в литры?
Литр=Килограмм/Плотность
Как перевести пропан-бутан из литров в килограммы?
Килограмм= Литр*Плотность
Как узнать плотность? Плотность пропан-бутана непостоянна. Мы для вас приготовили таблицу плотности пропан-бутановой смеси в зависимости от температуры воздуха (измеряемой в о С) и процентного соотношения пары двух газов в получаемой сжиженной смеси.
Мы для вас приготовили таблицу плотности пропан-бутановой смеси в зависимости от температуры воздуха (измеряемой в о С) и процентного соотношения пары двух газов в получаемой сжиженной смеси.
В верхней строке приведена температура окружающего воздуха (в о С), в левом столбце – процентное соотношение пропан-бутан (то есть, «90/10» означает, что смесь содержит 90% пропана и 10% бутана). На пересечении значений соотношения и температуры находится плотность смеси.
Газовый наполненный баллон объемом 50 литров будет содержать (при условии пропана и бутана в соотношении 70/30 и температуре 5 о С):
Сколько кубов в 50 литровом баллоне пропана
Re: А сколько кубов газа в 50л баллоне?Я правильно > считаю, что примерно 10?
> В баллоне 42л сжиженного газа.
В бытовом баллоне 50 литров получается 10 куб газа, проверено экпериментально (стоит счетчик). При условии заправки пустого баллона 40-41 литров газа.
Когда в сельский населённый пункт приходит газ, в него приходит цивилизация. Печное отопление, или отопление индивидуальное водяное с котлом на твёрдом топливе, – это не только романтическое потрескивание дров в топке. Отопление твёрдым топливом – это всегда копоть, дым и сажа, необходимость ежегодного перекрашивания потолков. А кроме неприятностей, связанных с постоянной грязью, необходимо ещё заготовить или приобрести и где-то хранить запас дров на целую зиму.
Печное отопление, или отопление индивидуальное водяное с котлом на твёрдом топливе, – это не только романтическое потрескивание дров в топке. Отопление твёрдым топливом – это всегда копоть, дым и сажа, необходимость ежегодного перекрашивания потолков. А кроме неприятностей, связанных с постоянной грязью, необходимо ещё заготовить или приобрести и где-то хранить запас дров на целую зиму.
К сожалению, не везде проведён природный трубопроводный газ. Во многих населённых пунктах жителям приходится довольствоваться газом в баллонах. И людей интересует, а сколько литров газа в 50-литровом баллоне?
Что такое бытовой газ
Вспомним основы школьной органической химии. Первым предельным углеводородом является метан. Молекула этого газа состоит из одного атома углерода, окружённого четырьмя атомами водорода.
Если слегка удлинить цепочку – вместо одного из атомов водорода «прицепить» один углерод, на оставшиеся три его связи присоединить атомы водорода, – получится следующий член семьи предельных углеводородов, этан.
Начиная с начала цепочки, имеем:
- метан СН4;
- этан С2Н6;
- пропан С3Н8;
- бутан С4Н10.
Последние два соединения – пропан и бутан – и являются содержимым бытовых газовых баллонов.
Физические свойства этих химических веществ
Пропан при нормальном атмосферном давлении является жидкостью в диапазоне температур от –187,7 до –42,1 °С. Ниже указанного промежутка пропан кристаллизуется, а выше, соответственно, переходит в газообразное состояние. У бутана этот диапазон: –138,3 … –0,5 °С. Как видим, температуры перехода в жидкость у обоих газов не намного ниже нуля, благодаря чему их достаточно легко сжижать, повышая давление.
Методы хранения газа
В быту используется, как правило, смесь пропан-бутан. В частных домах для хранения сжиженной смеси применяются стандартные 50-литровые газовые баллоны. Немного по-другому поступают при газоснабжении многоэтажек. Ну сколько литров газа в 50-литровом баллоне может поместиться?
Ну сколько литров газа в 50-литровом баллоне может поместиться?
А менять баллоны с 42 литрами газа (именно столько сжиженного газа хранится в баллоне) плюс вес самого баллона по всем этажам и квартирам… Поэтому в таких случаях во дворе дома устраивается, как правило, заземлённое хранилище, в которое специальными газовозами доставляется газовая смесь. В специальном устройстве она переводится в газообразную фазу и в таком виде поступает в бытовой трубопровод.
Объём газового баллона
Так сколько кубов газа в 50-литровом баллоне? Чтобы ответить на этот вопрос, необходимо определиться, какой газ нас интересует. Жидкой смеси газов в баллон заливается 42 литра. Но сколько это в килограммах, кубометрах? Плотность сжиженных: пропана – 0,528 кг/л, бутана – 601 кг/л.
Для того чтобы узнать, сколько литров газа в 50-литровом баллоне, произведём небольшие расчёты.
Но!! ! В 50-литровый под завязку не льют, баллон заполняется только на 85%, т. е. порядка 42,5 литров или 22 кг. Итого в 42,5 жидких литрах (22 кг жидкости) – 11,2 куба газа.
Итого в 42,5 жидких литрах (22 кг жидкости) – 11,2 куба газа.
то есть в полностью пустые баллоны должно быть залито заправщиком:
50 литровый баллон (22кг) – 42,5 литра = газа 23,16 кг (лето) или 21,97 кг газа (зима) = полный баллон 35,16 кг (лето) или 43,97 кг (зима).
27 литровый баллон (14,4кг) – 22,95 литра = газа 12,5 кг (лето) или 11,86 кг (зима) = полный баллон 26,9 кг (лето) или 26,26 кг (зима)
12 литровый баллон (9кг) – 10,2 литра = газа 5,56 кг (лето) или 5,27 кг (зима) = полный баллон 14,56 кг (лето) или 14,27 кг (зима)
5 литровый баллон (3кг) – 4,25 литра = газа 2,32 кг (лето) или 2,2 кг (зима) = полный баллон 5,32 кг (лето) или 5,2 кг (зима).
Важно: нормы заправки баллонов по объему могут отличаться на заправках, объем заправки газа (или вес) должен быть явно указан продавцом газа при указании стоимости заправки баллона, в этом случае вес можно аналогично пересчитать, согласно указанному объему заправки бытового газового баллона.
заправляемая газовая смесь летняя – 50% пропана + 50% бутана имеет теплотворную способность 6470 ккал/л или 11872 ккал/кг или 115 мДж/м3. Плотность 0,545 кг/литр. Плотность паровой фазы 2,2 кг/м куб.
Плотность 0,545 кг/литр. Плотность паровой фазы 2,2 кг/м куб.
заправляемая газовая смесь зимняя – 90% пропана + 10% бутана имеет теплотворную способность 6175 ккал/л или 11943 ккал/кг. Плотность 0,517 кг/л.
Какое количество кислорода в баллоне? | Пасс
Разные производители указывают количество кислорода баллоне от 6,0 м3 до 6,5 м3.
Согласно ГОСТ 5583-78 КИСЛОРОД ГАЗООБРАЗНЫЙ ТЕХНИЧЕСКИЙ И МЕДИЦИНСКИЙ (ссылка на документ) объем газообразного кислорода в баллоне (V) в кубических метрах при нормальных условиях вычисляют по формуле:
V = K1•V6,
- где V6 — вместимость баллона, дм3. В расчетах принимают среднюю статистическую величину вместимости баллонов не менее чем из 100 шт.;
- K1 — коэффициент для определения объема кислорода в баллоне при нормальных условиях, вычисляемый по формуле:
,
- где Р — давление газа в баллоне, измеренное манометром, кгс/см 2;
- 0,968 — коэффициент для пересчета технических атмосфер (кгс/см2) в физические;
- t — температура газа в баллоне, °С;
- Z — коэффициент сжигаемости кислорода при температуре t.

Коэффициент К1 при давлении в баллоне 150 кг/см2 и температуре 20 °С равен 0,156.
То есть в стандартном 40-ка литровом баллоне при давлении в баллоне 150 кг/см2 и температуре 20 0 С должно быть 40х0.156=6.24 м3 кислорода.
Однако среднестатистическая вместимость баллона при выборке не менее 100 реальных баллонов составляет 40,7-41 л.
То есть в стандартном 40-ка литровом баллоне при давлении в баллоне 150 кг/см2 и температуре 20 0 С должно быть 40,85х0.156=6.37 м3 кислорода.
Согласно ГОСТ 5583-78 КИСЛОРОД ГАЗООБРАЗНЫЙ ТЕХНИЧЕСКИЙ И МЕДИЦИНСКИЙ допустимая заправка баллона при 20 °С — 150 ± 5 кг/см
С учетом разрешенной степени наполнения баллонов в баллоне при 20 °С может находиться от 6, 12 до 6,53 м3 кислорода, что соответствует 8,14-8,69 кг. кислорода в баллоне.
Аналогично для аргона и азота.
Баллоны азотные 5л 10л 20л 40л 50л ГОСТ 949-73
Баллоны азотные, малого и среднего объема, из углеродистой и легированной стали ГОСТ 949-73. (Баллон N2)
(Баллон N2)
Баллон для азота окрашивается эмалью черного цвета, надпись » АЗОТ » желтого цвета.
Масса баллона под азот указана без вентилей, колпаков, колец и башмаков. Ориентировочная масса: колпака металлического — 1,8 кг; кольца — 0,3 кг; башмака — 5,2 кг
| Рабочее давление, МПа (кгс/см2) | Диаметр, мм | Баллоны АЗОТНЫЕ 50 литров | Баллоны АЗОТНЫЕ 40 литров | Баллоны АЗОТНЫЕ 20 литров | |||||||
| Сталь 45,Д | Сталь 30ХГСА | Сталь 45,Д | Сталь 30ХГСА | Сталь 45, Д | |||||||
| Длина, мм | Вес, кг | Длина, мм | Вес, кг | Длина, мм | Вес, кг | Длина, мм | Вес, кг | Длина, мм | Вес, кг | ||
| 14,7 (150) | 219 | 1685 | 71,3 | 1660 | 62,5 | 1370 | 58,5 | 1350 | 51,5 | 740 | 32,3 |
| 19,6 (200) | 219 | 1755 | 93,0 | 1660 | 62,5 | 1430 | 76,5 | 1350 | 51,5 | 770 | 42,0 |
| Рабочее давление, МПа (кгс/см2) | Диаметр, мм | Баллоны 12 литров АЗОТНЫЕ | Баллоны 10 литров АЗОТНЫЕ | Баллоны 8 литров АЗОТНЫЕ | Баллоны 5 литров АЗОТНЫЕ | Баллоны 4 литра АЗОТНЫЕ | Баллоны 2 литра АЗОТНЫЕ | ||||||
| Сталь 45,Д | Сталь 45,Д | Сталь 45,Д | Сталь 45,Д | Сталь 45, Д | Сталь 45,Д | ||||||||
| Длина, мм | Вес, кг | Длина, мм | Вес, кг | Длина, мм | Вес, кг | Длина, мм | Вес, кг | Длина, мм | Вес, кг | Длина, мм /диаметр, мм | Вес, кг | ||
| 14,7 (150) | 140 | 1020 | 17,6 | 865 | 13,0 | 710 | 12,4 | 475 | 8,5 | 400 | 7,3 | 330/108 | 3,7 |
|
Баллоны малого объема могут поставляться с плоским дном.
Освидетельствование азотных баллонов — каждые 5 лет.
Срок службы азотного баллона — 20 лет.
Гарантийный срок эксплуатации — 24 месяца со дня ввода в эксплуатацию
Объем азота в 40 литровом баллоне составляет 5,7м3, 6,7кг
Хотите купить азотный баллон ?
| ЗВОНИТЕ: | (8442) 780-530 | |
| (812) 309-73-72 | ||
| ПИШИТЕ: | [email protected] |
Узнаем как много литров газа в 50-литровом баллоне? Узнаем как много кубов газа в 50-литровом баллоне?
Когда в сельский населённый пункт приходит газ, в него приходит цивилизация. Печное отопление, или отопление индивидуальное водяное с котлом на твёрдом топливе, – это не только романтическое потрескивание дров в топке. Отопление твёрдым топливом – это всегда копоть, дым и сажа, необходимость ежегодного перекрашивания потолков. А кроме неприятностей, связанных с постоянной грязью, необходимо ещё заготовить или приобрести и где-то хранить запас дров на целую зиму.
А кроме неприятностей, связанных с постоянной грязью, необходимо ещё заготовить или приобрести и где-то хранить запас дров на целую зиму.
К сожалению, не везде проведён природный трубопроводный газ. Во многих населённых пунктах жителям приходится довольствоваться газом в баллонах. И людей интересует, а сколько литров газа в 50-литровом баллоне?
Вспомним основы школьной органической химии. Первым предельным углеводородом является метан. Молекула этого газа состоит из одного атома углерода, окружённого четырьмя атомами водорода.
- метан СН4;
- этан С2Н6;
- пропан С3Н8;
- бутан С4Н10.
Последние два соединения – пропан и бутан – и являются содержимым бытовых газовых баллонов.
Физические свойства этих химических веществ
Пропан при нормальном атмосферном давлении является жидкостью в диапазоне температур от –187,7 до –42,1 °С. Ниже указанного промежутка пропан кристаллизуется, а выше, соответственно, переходит в газообразное состояние. У бутана этот диапазон: –138,3 … –0,5 °С. Как видим, температуры перехода в жидкость у обоих газов не намного ниже нуля, благодаря чему их достаточно легко сжижать, повышая давление.
У бутана этот диапазон: –138,3 … –0,5 °С. Как видим, температуры перехода в жидкость у обоих газов не намного ниже нуля, благодаря чему их достаточно легко сжижать, повышая давление.
Методы хранения газа
В быту используется, как правило, смесь пропан-бутан. В частных домах для хранения сжиженной смеси применяются стандартные 50-литровые газовые баллоны. Немного по-другому поступают при газоснабжении многоэтажек. Ну сколько литров газа в 50-литровом баллоне может поместиться?
А менять баллоны с 42 литрами газа (именно столько сжиженного газа хранится в баллоне) плюс вес самого баллона по всем этажам и квартирам… Поэтому в таких случаях во дворе дома устраивается, как правило, заземлённое хранилище, в которое специальными газовозами доставляется газовая смесь. В специальном устройстве она переводится в газообразную фазу и в таком виде поступает в бытовой трубопровод.
Объём газового баллона
Так сколько кубов газа в 50-литровом баллоне? Чтобы ответить на этот вопрос, необходимо определиться, какой газ нас интересует.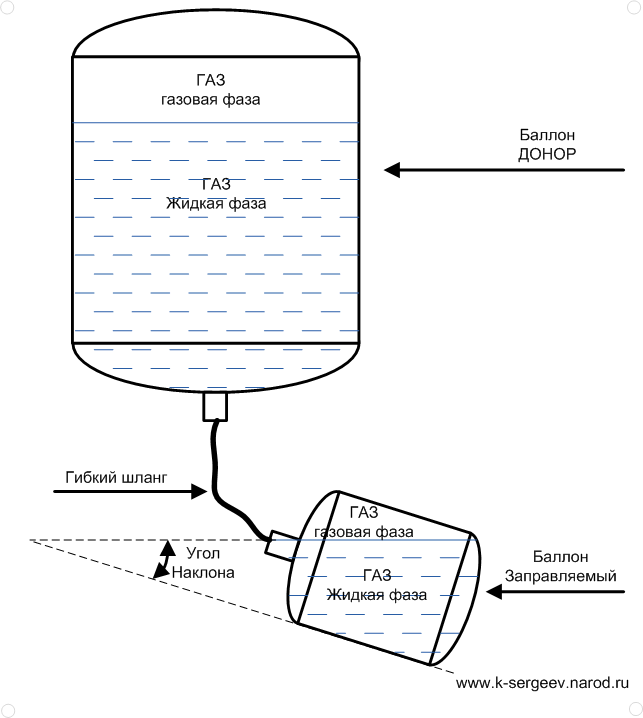 Жидкой смеси газов в баллон заливается 42 литра. Но сколько это в килограммах, кубометрах? Плотность сжиженных: пропана – 0,528 кг/л, бутана – 601 кг/л.
Жидкой смеси газов в баллон заливается 42 литра. Но сколько это в килограммах, кубометрах? Плотность сжиженных: пропана – 0,528 кг/л, бутана – 601 кг/л.
Для того чтобы узнать, сколько литров газа в 50-литровом баллоне, произведём небольшие расчёты.
Пропан | ||
Плотность жидкой фазы | 0,53 | кг/л |
Литров в баллоне | 42,00 | л |
Масса газа в баллоне | 22,18 | кг |
Плотность газообразной фазы | 1,87 | кг/м3 |
Объём, занимаемый 42 кг газа (1 баллон) | 22,44 | м3 |
Бутан | ||
Плотность жидкой фазы | 0,60 | кг/л |
Литров в баллоне | 42,00 | л |
Масса газа в баллоне | 25,24 | кг |
Плотность газообразной фазы | 2,52 | кг/м3 |
Объём, занимаемый 42 кг газа (1 баллон) | 16,67 | м3 |
Таким образом, сколько литров газа в 50-литровом баллоне, зависит от того, какой состав в него закачан. Если допустить, что баллон заполнен одним пропаном – 22,44 м3, бутаном – 16,67 м3. Но так как в быту используется смесь данных химических соединений, то показатель будет находиться где-то посередине.
Если допустить, что баллон заполнен одним пропаном – 22,44 м3, бутаном – 16,67 м3. Но так как в быту используется смесь данных химических соединений, то показатель будет находиться где-то посередине.
Если допустить, что пропан и бутан находятся в баллоне в равных долях, то ответ на вопрос, сколько газа в 50-литровом баллоне (м3) – около 20.
Меры безопасности при обращении с газовыми баллонами
- Никогда не удалять с баллонов таблички и этикетки.
- Не поднимать и не перемещать баллон, держась за вентиль.
- Утечки определять с помощью мыльного раствора, а не зажжённой спички.
- Вентиль баллона открывать плавно.
- Никогда не нагревать баллон.
- Самостоятельная перекачка (перелив) сжиженного газа в другие ёмкости запрещена.
Объем газового баллона. Максимальный объем пропановых бытовых баллонов
Сложно найти производство или домашнее хозяйство, где не применяют различные газы. На производственных площадках, газы применяют для резки и сварки металлов. В данной статье мы рассмотрим одну из характеристик газового баллона — объем.
В данной статье мы рассмотрим одну из характеристик газового баллона — объем.
В быту его применяют для приготовления еды и отопления жилья.
Для хранения и перевозки газов используют емкости, которые изготовлены из металла или композита.
Устройство газового баллона
Емкость для хранения и перевозки технического газа – это цилиндр определенной формы и объема, у которого в верхней части выполнено отверстие для установки вентиля.
В комплект поставки газовых емкостей входят:
- вентиль;
- сборный корпус, состоящий из обечайки, верхнего и нижнего дна. Для изготовления сосудов используют высококачественные стали или композитные материалы ;
- башмак – опора, предназначенная для того, чтобы емкость можно было установить в вертикальном положении;
- защитный колпак – элемент конструкции баллона, обеспечивающий защиту вентиля от повреждений при перевозке и эксплуатации.
Устройство газового баллона
Иногда в комплект поставки может входить редуктор. Так, называют устройство, регулирующее давление.
Так, называют устройство, регулирующее давление.
Газ из баллона выходит через вентиль. Это устройство состоит из корпуса, выполненного из металла, задвижки, управляющего штурвала. Корпус выполняют в виде тройника. Одна часть предназначена для установки его в емкость. Другая для закрепления штока регулирующего клапана и боковая для установки заглушки.
Задвижка включает в свой состав шток и клапан. Именно клапан управляет движением газа через вентиль. Шток служит для передачи крутящего момента от управляющего штурвала на клапан.
Внутренне содержание газового баллона
По сути, баллон напоминает обыкновенную зажигалку. Внутри емкости находится газ в двух агрегатных состояниях. В нижней части объема находиться жидкость, в верхней части газ.
Для того, чтобы знать какой газ в баллонах их окрашивают в разные цвета и наносят наименование технического газа. Например, баллоны с кислородом окрашивают в голубой цвет и наносят надпись «КИСЛОРОД».
Окрашивают в разные цвета и наносят наименование технического газа
Металлические и композитные газовые баллоны
На территории нашей страны действуют несколько ГОСТ регламентирующих технические условия к газовым емкостям. В частности, ГОСТ 949-73 регламентирует нормативы к стальным сосудам объемом от 0.4 до 50 литров и работающих с давлением от 9.8 до 19.6 МПа.
В частности, ГОСТ 949-73 регламентирует нормативы к стальным сосудам объемом от 0.4 до 50 литров и работающих с давлением от 9.8 до 19.6 МПа.
Металлические баллоны по праву считают оптимальным решением задачи хранения и перевозки технических газов. Для производства баллонов используют малоуглеродистые или легированные стальные сплавы. Баллоны выпускают с объемом от 5 до 50 литров и весом от 4 до 22 кг. Емкости с объемом в 50 литров необходимо устанавливать на улице в специально изготовленном для этого металлическом ящике. Емкости с меньшим объемом допустимо устанавливать в помещении, например, в гараже или ремонтной мастерской.
Кроме баллонов, изготовленных из стали для хранения и перевозки газа применяют изделия, выполненные из композита.
Они обладают следующими достоинствами:
- Малый вес, разница между баллонами одного объема может достигать 70%.

- Повышенная стойкость к ударным нагрузкам. Взрывобезопасность, даже под действием открытого огня.
- Конструкция композитного баллона выполнена таким образом, что практически утечка газа невозможна.
- Полимерные материалы, использованные при изготовлении баллона, исключают возникновение коррозии и образовании искр.
- Композитные сосуды обладают интересным внешним видом.
Для изготовления баллонов этого типа применяют стеклоткань и эпоксидные смолы.
Следует отметить, что с течением времени сосуд может изменить свой цвет, но это не влияет на его эксплуатационные свойства.
Для обеспечения безопасной эксплуатации полимерных сосудов приняты следующие меры:
- Установка клапана сброса излишнего давления.
- Установка плавящейся вставки.
При росте температуры газ начинает увеличиваться в объеме и в результате образуются его излишки. Они и создают лишнее давление на сосуд. Для устранения избытка давления предназначен предохранительный клапан. Он открывается по достижении определенного уровня давления.
Они и создают лишнее давление на сосуд. Для устранения избытка давления предназначен предохранительный клапан. Он открывается по достижении определенного уровня давления.
Под действием повышенной температуры, точно так же происходит рост давления внутри сосуда, в этом случае срабатывает плавкая вставка. Вставка расплавится и образует отверстие, через которое выходят излишки газа. Но, после срабатывания плавкой вставки, емкость подлежит утилизации.
Емкости разного объема, выполненные из композитных материалов, рассчитаны для работы при температуре от – 40 до +60 градусов.
Конструкция, объем и маркировка газовых сосудов
Конструкция, объем и маркировка газовых сосудов регламентирована ГОСТ 15860-84 (стальные баллоны), ГОСТ Р 55559-2013 (композитные сосуды).
Технические характеристики
Технические параметры сосуда для хранения и перевозки определенных объемов газа указывают в техническом паспорте. В частности, в нем должны быть отражают нижеприведенные данные:
Технические характеристики газовых баллонов
- Серийный номер, присвоенный сосуду на заводе-изготовителе;
- Фактический объем в литрах;
- Фактическая масса пустого сосуда в килограммах;
- Рабочее и тестовое давление в атмосферах;
- Дата выпуска и очередного переосвидетельствования;
- Шифр — клеймопредприятия-производителя или аттестованной лаборатории, где была выполнена переаттестация.

Масса и размер баллонов различной ёмкости
Один из самых широко применяемых газов – это, наверное, пропан. Его используют и в промышленности, и в быту. Для доставки этого газа используют и стальные, и композитные сосуды. Промышленность выпускает стальные сосуды объемом 5, 12, 27, 50 литров. Ёмкости с пропаном окрашивают в красный цвет, на боковой поверхности выполняют надпись «ПРОПАН», при этом высота букв должна быть не меньше 60 мм.
Вес металлического баллона с минимальным объемом в 5 литров составляет 4 кг.
Масса и размер баллонов различной ёмкости
Сосуды имеют следующие габариты от 200 до 299 мм, при высоте от 290 до 930 мм.
Объем газового баллона из композитных материалов, предназначенного для пропана, составляет от 0.5 до 150 литров с рабочим давлением 2 МПа. В тоже же время баллоны, применяемые для автомобильного ГБО, работают под давлением до 30 МПа. Объем такого газового баллона составляет от 47 до 180 литров. Диаметр таких баллонов составляет от 326 до 398 мм, длина составляет от 840 до 2000 мм. Габариты баллонов зависят от объема сосуда.
Габариты баллонов зависят от объема сосуда.
Количество газа в бытовом баллоне 50 , 27, 12 , 5 литров
Существуют определенные соотношения между объемом баллона и его весом. Так, в баллоне на 50 литров может храниться 21,2 кг, а в пятилитровом сосуде находится 2 кг газа.
Количество газа в бытовом баллоне 50 , 27, 12 , 5 литров
Правила безопасной эксплуатации газовых баллонов
При эксплуатации емкостей со сжатым газом необходимо соблюдать определенные правила безопасности.
Перемещение газового баллона
В частности, нельзя допускать:
- Утечек газа через стыки и резьбовые соединения и образования взрывоопасной смеси с воздухом.
- Теплового воздействия на емкости, которое может привести к росту объема газа и давления внутри баллона.
- Механических воздействий ударного типа, которые могут повредить стенки емкости.
Правила безопасности требуют, чтобы перевозка емкостей проводилась с установленными на них защитными колпаками.
Сосуды с газом могут перевозиться с места на место в горизонтальном или вертикальном положении. Но при этом необходимо обеспечить защиту от самопроизвольного перемещения емкостей внутри кузова.
Недопустимо бросать емкости с газом ударять их о твердые предметы.
Правила безопасной эксплуатации газовых баллонов
Газовую емкость в жилом помещении хранить недопустимо. В идеале сосуд с газом должен храниться в отдельно стоящем железном ящике.
Хранение газовых баллонов на производстве
Здания для хранения емкостей с техническим газом на производственной площадке должны быть не выше одного этажа и при этом не иметь чердака. Такие сооружения должны быть выполнены из негорючих материалов. Окна и двери должны быть оснащены матовыми или равномерно окрашенными в белый цвет стеклами. Это необходимо для рассеивания прямого солнечного цвета.
Горизонтальное хранение газовых баллонов
Помещения, где хранят емкости с газом, должны быть оснащены постоянно действующей вентиляцией. Правила хранения газовых баллонов требуют того, чтобы на складе где осуществляют хранение газов необходимо постоянно проверять качество воздуха, на предмет наличия посторонних примесей. При достижении в воздухе опасной концентрации газов помещение необходимо проверить, а емкости с газом необходимо со склада удалить.
В процессе эксплуатации баллонов недопустимо:
- Эксплуатировать баллоны с просроченным сроком испытания, на их поверхности нет установочных клейм, поврежден вентиль или корпус.
- Самостоятельное выполнение ремонта или окрашивание баллонов и установленной на них арматуры.
- Отогревать редуктора с применением открытого пламени. Эту операцию можно выполнять только с применением горячей воды.
- Работать вблизи баллонов в промасленной одежде и пр.
Можно ли по давлению определить остаток сжиженного газа в пропан-бутановом баллоне
К сожалению, нет. Дело в том, что давление в баллоне определяет пар, находящийся над жидкостью, и оно имеет постоянное значение вне зависимости объема последней.
Весовая установка для наполнения газового баллона
Для того, чтобы определить остаток газа в баллоне его необходимо взвесить.
Принцип подключения газового баллона к плите
Правила безопасности, которые необходимо изучить перед подключением газового баллона к плите, изложены в СНиП 42-01-2002. Перед тем как подключать емкость к газовой плите необходимо выполнить несколько подготовительных операций.
Весь процесс подключения должен проходить при тщательном осмотре каждой детали:
- Осмотреть все детали, которые участвуют в подключении. На них, особенно на местах резьбовых соединений не должно быть загрязнений и следов коррозии.
- Особо внимательно необходимо осмотреть шланг. Вообще, при подключении целесообразно использовать специальной купленный для этого рукав. Кроме того, что он должен быть строго определенной длины, на его поверхности не должно быть трещин и других дефектов. Кроме того, при сборке его недопустимо перекручивать.
Подключение газового баллона к плите производят в следующем порядке:
- Установить газовую плиту на заранее определенное место. Емкость, располагают или в другом помещении или на расстоянии до корпуса плиты не менее одного метра.
- Емкость должен быть установлен на ровное место, для повышения устойчивости баллона целесообразно установить для него ограждение из реек.
- Перед тем как присоединить шланг к плите необходимо приготовить фум-ленту. Намотать ее на резьбу и присоединить шлаг ко входу на плиту.
- Перед тем как подсоединить плиту к баллону, на него необходимо установить редуктор. В народе это устройство называют «лягушкой».
- Подключение газовой плиты к баллону выполняют с помощью рукава.
Все соединения должны быть выполнены герметичны.
Принцип подключения газового баллона к плите
После того как система собрана, необходимо проверить качество сборки. Самый простой способ – это использование мыльной пены. То есть, на места соединения необходимо нанести мыльную пену и при появлении пузырей необходимо разобрать соединение и собрать его по новой.
Особенности поведения газовых баллонов в очаге пожара
Если емкость с газом попадает в очаг пожара, происходит его нагревание. В результате жидкость, находящаяся в баллоне, закипает и приводит к росту давления. Кроме того, нагрев баллона происходит неравномерно и это ослабляет его прочность. Все это приводит к разрыву корпуса баллона.
Кстати, к особенностям поведения газовых баллонов в очаге возгорания можно отнести следующее — если емкость объем в 50 литров попадет в очаг пожара, то разгерметизация и взрыв произойдет через 3,5 минуты. При этом осколки могут разлетаться на расстояние до 200 метров.
Сроки службы газовых баллонов
В ГОСТ 15860 срок службы газовых баллонов с рабочим давлением 1,6 МПа, определен в 40 лет, при этом он должен проходить через переосвидетельствование.
Маркировка по срокам службы газовых баллонов
Между тем существует понятие – эксплуатационный срок, его ни в коем случае нельзя путать с гарантийным. Как правило, он составляет 20 лет.
Производители устанавливают эксплуатационные сроки на основании Приказа No 485, в нем вынесена рекомендация устанавливать такой срок в 20 лет.
Справочник молодого сварщика и дачника — Записки странствующего слесаря
Сколько газа в баллонеКислород, аргон, гелий, сварочные смеси: 40 литров баллон при 150 атм — 6 куб.м
Ацетилен: 40 литров баллон при 19 атм — 4,5 куб.м
Углекислота: 40 литров баллон — 24 кг — 12 куб.м
Пропан: 50 литров баллон — 42 литра жидкого газа — 21 кг — 10 куб.м.
Давление кислорода в баллоне в зависимости от температуры
-40С — 105 атм
-20С — 120 атм
0С — 135 атм
+20С — 150 атм (номинал)
+40С — 165 атм
Проволока сварочная Св-08 и производные от неё, вес 1 километра по длине
0,6 — 2,222 кг
0,8 — 3,950 кг
1,0 — 6,173 кг
1,2 — 8,888 кг
Калорийность (теплотворная способность) сжиженного и природного газа
Природный газ — 8500 ккал/м3
Сжиженный газ — 21800 ккал/м3
Примеры использования вышеприведенных данных
Вопрос: На сколько хватит газа и проволоки при сварке полуавтоматом с кассетой проволоки 0,8 мм весом 5 кг и баллона с углекислотой объемом 10 литров?
Ответ: Сварочная проволока СВ-08 диаметром 0,8 мм весит 3,950 кг 1 километр, значит на кассете 5 кг примерно 1200 метров проволоки. Если средняя скорость подачи для такой проволоки 4 метра в минуту, то кассета уйдет за 300 минут. Углекислоты в «большом» 40-литровом баллоне 12 кубометров или 12000 литров, если пересчитать на «маленький» 10-литровый баллон, то в нём углекислоты будет 3 куб. метра или 3000 литров. Если расход газа на продувку 10 литров в минуту, то 10-литрового баллона обязано хватить 300 минут или на 1 кассету проволоки 0,8 весом 5 кг, или «большого» баллона 40 литров на 4 кассеты по 5 кг.
Вопрос: Хочу поставить на даче газовый котел и отапливаться от баллонов, на сколько будет хватать одного баллона?
Ответ: В 50-литровом «большом» пропановом баллоне 21 кг сжиженного газа или 10 кубометров газа в газообразном виде. Находим данные котла, например возьмем очень распространенный котел АОГВ-11,6 мощностью 11,6 кВт и рассчитанный на отопление 110 кв. метров. На сайте ЖМЗ указан расход сразу в килограммах в час для сжиженного газа — 0,86 кг в час при работе на полную мощность. 21 кг газа в баллоне делим на 0,86 кг/час = 18 часов непрерывного горения такого котла на 1 баллоне, реально это будет происходить, если на улице -30С при стандартном доме и обычном требовании к температуре воздуха в нем, а если на улице будет всего всего -20С, то 1 баллона будет хватать на 24 часа (сутки). Можно сделать вывод, что чтоб отапливать обычный домик в 110 кв. метров баллонным газом в холодные месяцы года нужно примерно 30 баллонов в месяц. Нужно помнить, что в связи с разной теплотворной способностью сжиженного и природного газа расход сжиженного и природного газа при одной и той же мощности для котлов разный. Для перехода с одного вида газа на другой в котлах обычно нужно менять жиклеры / форсунки. Делая расчеты обязательно учитывайте это и берите данные расхода именно для котла с жиклерами под правильный газ.
Полностью материал тут: http://www.udarnik-truda.ru/workshop/welding/welding.htm
| Размер цилиндра | 47AL | 30AL | 16AL | 7AL | 3AL | 1AL |
| Спецификация DOT | 3AL | 3AL | 3AL | 3AL | 3AL | 3AL |
| Рабочее давление (фунт / кв. Дюйм) | 2216 | 2015 | 2216 | 2216 | 2015 | 2216 |
| Приблизительная вместимость (кубические футы) | 244 | 141 | 83 | 31 | 8 | 5 |
| Приблизительная вместимость (литры) | 6909 | 3993 | 2350 | 878 | 227 | 142 |
| Внешний диаметр (дюймы) | 9.8 | 8 | 7,25 | 6,9 | 4,4 | 3,2 |
| Высота (дюймы) | 51,9 | 47,9 | 33 | 15,6 | 10,5 | 11,7 |
| Масса тары (фунт.) | 90 | 48 | 30 | 15 | 3,5 | 2,3 |
| Внутренний водный объем (кубические дюймы) | 2831 | 1800 | 958 | 360 | 103 | 61 |
| Внутренний объем воды (литры) | 46.4 | 29,3 | 15,7 | 5,9 | 1,7 | 1 |
Кислородный баллон на 10 кубических метров
AirLocus обеспечивает отличные эксплуатационные характеристики кислородных баллонов объемом 10 кубических метров для промышленного и медицинского применения. Наши кислородные баллоны объемом 10 кубических метров спроектированы, изготовлены и проверены в соответствии с международными стандартами.Кислородные баллоны объемом 10 кубических метров изготовлены из высокопрочной стали или алюминия марки 6061 и имеют характеристики одинаковой высоты, четкой гравировки, длительного срока службы и т. Д. По любым вопросам, связанным с кислородным баллоном на 10 кубических метров, обращайтесь к нам.
50 л 200 бар кислородный баллон | |||
Тип | ISO232-50-200A | Внешний диаметр | 232 мм |
Объем воды | 50L | Высота без клапана | 1425 мм |
Рабочее давление | 200 бар | мин.толщина стенки | 5,2 мм |
Испытательное давление | 300 бар | Масса без клапана | 50,6 кг |
Производственный стандарт | ISO9809-1 | Материал | 34CrMo4 |
50 л 200 бар кислородный баллон | |||
Тип | ISO232-50-200B | Внешний диаметр | 232 мм |
Объем воды | 50L | Высота без клапана | 1450 мм |
Рабочее давление | 200 бар | мин.толщина стенки | 5,8 мм |
Испытательное давление | 300 бар | Масса без клапана | 56,3 кг |
Производственный стандарт | ISO9809-1 | Материал | 34CrMo4 |
50 л 200 бар кислородный баллон | |||
Тип | ISO229-50-200A | Внешний диаметр | 229 мм |
Объем воды | 50L | Высота без клапана | 1505 мм |
Рабочее давление | 200 бар | мин.толщина стенки | 6,2 мм |
Испытательное давление | 300 бар | Масса без клапана | 64.0 кг |
Производственный стандарт | ISO9809-1 | Материал | Трубка 30CrMo |
50 л 200 бар кислородный баллон | |||
Тип | ISO229-50-200B | Внешний диаметр | 229 мм |
Объем воды | 50L | Высота без клапана | 1510 мм |
Газовый баллон с аргоном, 7-метровый куб, 250 рупий / кубический метр Rajesh Gas Agencies
Аргоновый газовый баллон, 7-метровый куб, 250 рупий / кубический метр Rajesh Gas Agencies | ID: 19283055448Спецификация продукта
| Размер упаковки | 7-метровый куб |
| Материал | Низкоуглеродистая сталь |
| Чистота (%) | 95-99 |
| Объем баллона с аргоном | 10-50 л |
Описание продукта
Благодаря большому опыту в этой области, мы способствуем предложению Баллонов с аргоном ?? нашим клиентам.
Заинтересовал этот товар? Получите последнюю цену от продавца
Связаться с продавцом
Изображение продукта
О компании
Год основания 1992
Юридический статус Фирмы Физическое лицо — Собственник
Характер бизнеса Оптовый торговец
Количество сотрудников До 10 человек
Годовой оборот1-2 крор
Участник IndiaMART с февраля 2011 г.
GST27ABGPA3660F1Z1
Основанная в году 1992 по адресу Lakadganj, Nagpur, Maharashtra , мы « Rajesh Gas Agencies » — это индивидуальное предприятие (индивидуальное лицо) , основанное на и являющееся ведущим оптовым продавцом газовых баллонов с аргоном и кислородом. , Баллон с азотом, баллон с жидким азотом, баллон с растворенным ацетиленом, баллон с газом для диоксида углерода, промышленный баллон с кислородом и . Наша продукция пользуется большим спросом благодаря первоклассному качеству, бесшовной отделке, разнообразию рисунков и доступным ценам. Кроме того, мы гарантируем своевременную доставку этих продуктов нашим клиентам, благодаря чему мы приобрели огромную клиентскую базу на рынке.Видео компании
Вернуться к началу 1 Есть потребность?
Получите лучшую цену
Есть потребность?
Получите лучшую цену
Факты о гелии — Введение
Извлечение и сжижение гелия
На рисунке показано изменение объема гелия при различных давлениях и температурах в типичном баллоне для хранения газа объемом 50 литров, газовом мешке объемом 10 м³ (равно 10.000 литров) и транспортный дьюар объемом 100 литров, в который заправлено всего 12,5 литров жидкого гелия.
Что делает гелий таким уникальным?
- Редкий на Земле, но второй по распространенности элемент во Вселенной после водорода
- Образуется в земной коре в результате радиоактивного распада He2 +
- Наибольшие количества можно найти в природном газе (от 0,3 до 2,7%)
- Существуют два стабильных изотопа: 4He и 3He
- Назван в честь Гелиоса, греческого бога солнца
Применение гелия
- Гелий-кислородные смеси (80:20) в медицине
- Газ для профессиональных водолазов («Тримикс», «Гелиокс»)
- Пищевая промышленность (E939)
- Гелиевые шары
- Сварка
- Инертный (защитный) газ
- Газ-носитель для газовой хроматографии
- Проверка герметичности
- Лазеры (He-Ne-лазер, He-Cd-лазер)
- Сжатый газ вместо воздуха (Формула 1)
- Криогеника
Расход гелия
Относительные количества гелия, потребленные различными способами в США в 2016 году.График использует данные USGS. Он показывает, что почти 1/3 всего гелия в США использовалась в криогенной форме, например в виде жидкого гелия при температурах охлаждения до 4,2 К и ниже.
Мировое потребление гелия в миллионах кубических метров (источник)
Зачем перерабатывать гелий?
Гелий — самый распространенный элемент в космосе. Однако здесь, на Земле, его можно найти лишь в небольшом количестве в некоторых месторождениях природного газа.
Попав в воздух, он диффундирует в стратосферу и становится недоступным.
Переработка гелия:
Экономия затрат — Текущие затраты на рекуперацию намного меньше, чем при покупке жидкого гелия.
Делает независимо от внешних поставщиков — Гелий всегда доступен на месте.
Помогает контролировать качество — каждая новая партия внешнего гелия может быть загрязнена водородом, что приводит к неисправности криостатов.
Помогает защитить окружающую среду — Сохраняется ограниченный ресурс гелия.
Инструмент компоновки для извлечения гелия
Правильный размер вашей регенерации гелия поможет вам максимизировать эффективность регенерации вашей установки по извлечению жидкого гелия. Этот инструмент даст вам первое представление о том, какое восстановление вам следует рассмотреть с вашими предварительными условиями. Просто введите количество жидкого гелия (LHe) в литрах, которое вы переносите во время максимальной перекачки, чтобы получить максимальную конфигурацию системы восстановления, которая вам нужна. Также укажите потери за перевод в литрах.Обычно они составляют от 20 до 30% от общего перенесенного жидкого гелия.
Перейти к инструменту компоновки восстановления гелия
Для точной оценки вашей ситуации вам также необходимо ввести время, необходимое для заполнения ваших криостатов жидким гелием (время переноса), и количество жидкого гелия, которое вы хотите хранить в виде газа в вашей системе рекуперации. Указанный результат будет предложенным количеством баллонов с гелием объемом 1000 литров, находящихся под давлением до 5 бар. При значении выше 5 мы предлагаем использовать систему восстановления высокого давления (HPR), поскольку площадь основания соответствующей системы восстановления среднего давления (MPR) будет намного больше.Если это нежелательно, мы предлагаем пересмотреть количество хранимого жидкого гелия как газа.
Если потеря газообразного гелия обозначена как отрицательное значение, то ее можно рассматривать как истинную потерю. Положительное значение означает, что поток газообразного гелия может быть собран, если количество газовых баллонов равно или превышает рассчитанное количество.
Для регенерации высокого давления рассчитанные значения представляют собой размер газового мешка в кубических метрах и количество газовых баллонов объемом 50 литров (давление 200 бар).
Предполагается, что все расчеты помогут понять, какое решение для восстановления лучше всего соответствует вашим требованиям. Пожалуйста, свяжитесь с нами для получения дополнительной информации и полной настройки конфигурации.
Как перерабатывается гелий?
Типичная малогабаритная установка по извлечению и сжижению гелия работает со следующими этапами обработки:
Коллекция
Газообразный гелий собран из прибора. Обдумайте тип используемого комплекта для восстановления и способы защиты оборудования от воздействия раствора для восстановления.
Хранилище
Прямое восстановление
Без хранения — один инструмент
Среднее давление
Гелий хранится в стальных резервуарах под давлением 5 бар.
Высокое давление
Гелий накапливается в баллоне и хранится в стальных баллонах под давлением 200 бар.
Очистка
Inline
Очистители, такие как осушители и геттеры
Ловушка для жидкого азота
Адсорбция на угле при 77 К
Криогенный очиститель
Работает при 10-25 К — автоматизированное решение
Сжижение
Компактный переносной ожижитель с криокулером Gifford-McMahon.
Производит 10-30 литров жидкого гелия в сутки.
Конфигурации хранилища
Прямое восстановление
Базовая конфигурация
A — ожижитель лабораторного размера
B — гелиевый компрессор
C — регулятор давления рекуперации
D — блок питания
X — криогенный прибор
Pro:
- Простота установки и использования
- Минимум необходимого места
- Дешевле
- Возможность модернизации до MP или H
Contra:
- Ограниченная степень извлечения (70-80%) из-за потерь при переносе
Восстановление среднего давления
Восстановление с использованием стальных резервуаров для хранения гелия (8-10бар)
A — ожижитель лабораторного размера
B — гелиевый компрессор
C — бустерная ступица с буферным баком
D — очиститель
E — резервуары для хранения
F — регулятор давления рекуперации
X — криогенный прибор
Pro:
- Идеально для одного или двух инструментов
- Высокая эффективность (> 95%)
Contra:
Восстановление высокого давления
Восстановление с баллонами для хранения гелия (200 бар)
A — ожижитель лабораторного размера
B, D — гелиевые компрессоры
C — криогенный очиститель
E — газовый мешок с контроллером
F — компрессор высокого давления
G — связка баллонов-накопителей
H — регулятор давления рекуперации
X — криогенный прибор (s)
Pro:
- Универсальный, настраиваемый и масштабируемый
- Подходит для любого типа потребителей гелия
- Очень высокий КПД (> 98%)
Contra:
- Сравнительно более высокие затраты
- Требуется много места (для гелиевого шара)
Полезные ссылки
Документ Gasworld: глобальный гелиевый саммит 2.0
Подробная информация о дефиците гелия
Закон об идеальном газе | Физика
Цели обучения
К концу этого раздела вы сможете:
- Сформулируйте закон идеального газа, используя молекулы и моль.
- Используйте закон идеального газа для расчета изменения давления, температуры, объема или количества молекул или молей в заданном объеме.
- Используйте число Авогадро для преобразования числа молекул в число молей.
Рис. 1. Воздух внутри воздушного шара, летящего над Путраджайей, Малайзия, горячее окружающего воздуха. В результате воздушный шар испытывает подъемную силу, толкающую его вверх. (Источник: Кевин По, Flickr)
В этом разделе мы продолжаем исследовать термическое поведение газов. В частности, мы исследуем характеристики атомов и молекул, из которых состоят газы. (Большинство газов, например азот, N 2 , и кислород, O 2 , состоят из двух или более атомов.Мы в первую очередь будем использовать термин «молекула» при обсуждении газа, потому что этот термин также может быть применен к одноатомным газам, таким как гелий.)
Газы легко сжимаются. Мы можем увидеть доказательства этого в Таблице 1 в Термическом расширении твердых тел и жидкостей, где вы заметите, что газы имеют наибольших коэффициентов объемного расширения. Большие коэффициенты означают, что газы расширяются и сжимаются очень быстро при изменении температуры. Кроме того, вы заметите, что большинство газов расширяются с той же скоростью или имеют ту же β .Это поднимает вопрос о том, почему все газы должны действовать почти одинаково, когда жидкости и твердые тела имеют сильно различающиеся скорости расширения.
Ответ заключается в большом разделении атомов и молекул в газах по сравнению с их размерами, как показано на рисунке 2. Поскольку атомы и молекулы имеют большие расстояния, силы между ними можно игнорировать, за исключением случаев, когда они сталкиваются друг с другом во время столкновений. . Движение атомов и молекул (при температурах значительно выше температуры кипения) происходит быстро, так что газ занимает весь доступный объем, и газы расширяются быстро.Напротив, в жидкостях и твердых телах атомы и молекулы расположены ближе друг к другу и весьма чувствительны к силам между ними.
Рис. 2. Как показано, атомы и молекулы в газе обычно широко разделены. Поскольку силы между ними на этих расстояниях довольно малы, свойства газа больше зависят от количества атомов в единице объема и от температуры, чем от типа атома.
Чтобы получить некоторое представление о том, как давление, температура и объем газа связаны друг с другом, подумайте, что происходит, когда вы закачиваете воздух в изначально спущенную шину.Сначала объем шины увеличивается прямо пропорционально количеству впрыскиваемого воздуха без значительного увеличения давления в шине. Как только шина расширилась почти до своего полного размера, стенки ограничивают объемное расширение. Если продолжать закачивать в него воздух, давление возрастает. Давление будет еще больше увеличиваться, когда автомобиль движется, а шины двигаются. Большинство производителей указывают оптимальное давление в шинах для холодных шин. (См. Рисунок 3.)
Рис. 3. (a) Когда воздух закачивается в спущенную шину, его объем сначала увеличивается без значительного увеличения давления.(b) Когда шина заполнена до определенной точки, стенки шины сопротивляются дальнейшему расширению, и давление увеличивается с увеличением количества воздуха. (c) Когда шина накачана, ее давление увеличивается с температурой.
При комнатной температуре столкновениями между атомами и молекулами можно пренебречь. В этом случае газ называется идеальным газом, и в этом случае соотношение между давлением, объемом и температурой задается уравнением состояния, называемым законом идеального газа.
Закон об идеальном газе
Закон идеального газа гласит, что PV = NkT , где P — абсолютное давление газа, V — объем, который он занимает, N — количество атомов и молекул в газа, а T — его абсолютная температура.Константа k называется постоянной Больцмана в честь австрийского физика Людвига Больцмана (1844–1906) и имеет значение k = 1,38 × 10 −23 Дж / К.
Закон идеального газа может быть выведен из основных принципов, но первоначально он был выведен из экспериментальных измерений закона Чарльза (объем, занимаемый газом, пропорционален температуре при фиксированном давлении) и закона Бойля (для фиксированной температуры, произведение PV является константой).В модели идеального газа объем, занимаемый его атомами и молекулами, составляет ничтожную долю от V . Закон идеального газа описывает поведение реальных газов в большинстве условий. (Обратите внимание, например, что N — это общее количество атомов и молекул, независимо от типа газа.)
Давайте посмотрим, как закон идеального газа согласуется с поведением заполнения шины, когда она накачивается медленно и температура постоянна. Сначала давление P по существу равно атмосферному давлению, а объем V увеличивается прямо пропорционально количеству атомов и молекул N , помещенных в шину.Как только объем шины остается постоянным, уравнение PV = NkT предсказывает, что давление должно увеличиваться пропорционально числу N атомов и молекул.
Пример 1. Расчет изменений давления из-за изменений температуры: давление в шинах
Предположим, шина вашего велосипеда полностью накачана, с абсолютным давлением 7,00 × 10 5 Па (манометрическое давление чуть менее 90,0 фунтов / дюйм 2 ) при температуре 18,0 ° C.Какое давление будет после повышения температуры до 35,0ºC? Предположим, что нет заметных утечек или изменений объема.
Стратегия
Давление в шине меняется только из-за изменения температуры. Сначала нам нужно определить, что мы знаем и что мы хотим знать, а затем определить уравнение, которое нужно решить для неизвестного.
Известно начальное давление P 0 = 7,00 × 10 5 Па, начальная температура T 0 = 18.0ºC, а конечная температура T f = 35,0ºC. Мы должны найти конечное давление P f . Как мы можем использовать уравнение PV = NkT ? На первый взгляд может показаться, что информации недостаточно, потому что объем V и количество атомов N не указаны. Что мы можем сделать, так это использовать уравнение дважды: P 0 V 0 = NkT 0 и P f V f = NkT f .Если мы разделим P f V f на P 0 V 0 , мы можем придумать уравнение, которое позволяет нам решить для P f .
[латекс] \ displaystyle \ frac {P _ {\ text {f}} V _ {\ text {f}}} {P_0V_0} = \ frac {N _ {\ text {f}} kT _ {\ text {f}}} {N_0kT_0} \\ [/ latex]
Поскольку громкость постоянна, V f и V 0 одинаковы, и они уравновешиваются. То же самое верно для N f и N 0 и k , что является константой.Следовательно,
[латекс] \ displaystyle \ frac {P _ {\ text {f}}} {P_0} = \ frac {T _ {\ text {f}}} {T_0} \\ [/ latex]
Затем мы можем изменить это, чтобы решить для P f : [latex] P _ {\ text {f}} = P_0 \ frac {T _ {\ text {f}}} {T_0} \\ [/ latex] , Где температура должна быть в единицах кельвина, потому что T 0 и T f являются абсолютными температурами.
Решение
Преобразование температуры из Цельсия в Кельвин:
T 0 = (18.5 \ text {Pa} \\ [/ latex]
Обсуждение
Конечная температура примерно на 6% выше исходной температуры, поэтому конечное давление также примерно на 6% больше. Обратите внимание, что в законе идеального газа должны использоваться абсолютное давление и абсолютная температура .
Подключение: домашний эксперимент — охлаждение воздушного шара
Надуйте баллон при комнатной температуре. Оставьте надутый баллон в холодильнике на ночь.Что происходит с воздушным шаром и почему?
Пример 2. Расчет количества молекул в кубическом метре газа
Сколько молекул содержится в типичном объекте, таком как газ в шине или вода в напитке? Мы можем использовать закон идеального газа, чтобы дать нам представление о том, насколько велик обычно N .
Вычислите количество молекул в кубическом метре газа при стандартной температуре и давлении (STP), которые определены равными 0ºC и атмосферному давлению.
Стратегия
Поскольку давление, объем и температура указаны, мы можем использовать закон идеального газа PV = NkT , чтобы найти N .{25} \ text {молекулы} \\ [/ latex]
Обсуждение
Это число, несомненно, велико, учитывая, что газ — это в основном пустое пространство. N огромен даже в небольших объемах. Например, 1 см 3 газа в STP содержит 2,68 × 10 19 молекул. Еще раз отметим, что N одинаков для всех типов или смесей газов.
Родинки и число Авогадро
Иногда при измерении количества вещества удобно работать с единицей, отличной от молекул. моль (сокращенно моль) определяется как количество вещества, которое содержит столько атомов или молекул, сколько атомов имеется ровно в 12 граммах (0,012 кг) углерода-12. Фактическое количество атомов или молекул в одном моле называется числом Авогадро ( N A ), по признанию итальянского ученого Амедео Авогадро (1776–1856). Он разработал концепцию мола, основываясь на гипотезе о том, что равные объемы газа при одинаковом давлении и температуре содержат равное количество молекул.То есть количество не зависит от типа газа. Эта гипотеза подтвердилась, и значение числа Авогадро составляет N A = 6,02 × 10 23 моль -1 .
Число Авогадро
Один моль всегда содержит 6,02 × 10 23 частиц (атомов или молекул), независимо от элемента или вещества. Моль любого вещества имеет массу в граммах, равную его молекулярной массе, которую можно вычислить из атомных масс, указанных в периодической таблице элементов.
N A = 6,02 × 10 23 моль −1
Рис. 4. Насколько велика родинка? На макроскопическом уровне один моль мячей для настольного тенниса покроет Землю на глубину около 40 км.
Проверьте свое понимание
Активным ингредиентом таблетки Тайленола является 325 мг ацетаминофена (C 8 H 9 NO 2 ). Найдите количество активных молекул парацетамола в одной таблетке.
Решение
Сначала нам нужно вычислить молярную массу (массу одного моля) ацетаминофена.{-3} \ text {moles} \\ [/ latex]
Затем используйте число Авогадро, чтобы вычислить количество молекул.
N = (2,15 × 10 −3 моль) (6,02 × 10 23 молекул / моль) = 1,30 × 10 21 молекул
Пример 3. Расчет молей на кубический метр и литров на моль
Вычислите следующее:
- Количество молей в 1,00 м 3 газа на СТП
- Количество литров газа на моль.3} = 22,5 \ text {л / моль} \\ [/ latex]
Обсуждение
Это значение очень близко к принятому значению 22,4 л / моль. Небольшая разница связана с ошибками округления, вызванными использованием трехзначного ввода. Опять же, это число одинаково для всех газов. Другими словами, он не зависит от газа.
(средняя) молярная масса воздуха (приблизительно 80% N 2 и 20% O 2 составляет M = 28,8 г. Таким образом, масса одного кубического метра воздуха равна 1,28 кг.Если гостиная имеет размеры 5 м × 5 м × 3 м, масса воздуха внутри комнаты составляет 96 кг, что является типичной массой человека.
Проверьте свое понимание
Плотность воздуха при стандартных условиях ( P = 1 атм и T = 20ºC) составляет 1,28 кг / м 3 . При каком давлении будет плотность 0,64 кг / м 3 , если температура и количество молекул остаются постоянными?
Решение
Лучший способ подойти к этому вопросу — подумать о том, что происходит.Если плотность упадет до половины от исходного значения и никакие молекулы не потеряны, объем должен удвоиться. Если мы посмотрим на уравнение PV = NkT , мы увидим, что при постоянной температуре давление обратно пропорционально объему. Следовательно, если объем увеличится вдвое, давление должно упасть до половины своего первоначального значения, и P f = 0,50 атм.
Пересмотр закона об идеальном газе с использованием молей
Очень распространенное выражение закона идеального газа использует количество молей, n , а не количество атомов и молекул, N .Начнем с закона идеального газа, PV = NkT , умножим и разделим уравнение на число Авогадро N A . Это дает [latex] PV = \ frac {N} {N _ {\ text {A}}} N _ {\ text {A}} kT \\ [/ latex].
Обратите внимание, что [латекс] n = \ frac {N} {N _ {\ text {A}}} \\ [/ latex] — это количество молей. Мы определяем универсальную газовую постоянную R = N A k и получаем закон идеального газа в молях.
Закон идеального газа (в молях)
Закон идеального газа (в молях): PV = nRT .
Числовое значение R в единицах СИ составляет R = N A k = (6,02 × 10 23 моль −1 ) (1,38 × 10 −23 Дж / К ) = 8,31 Дж / моль · К.
В прочих единицах,
R = 1,99 кал / моль · K
R = 0,0821 л · атм / моль · K
Вы можете использовать любое значение R , наиболее подходящее для конкретной задачи.
Пример 4. Расчет количества молей: газ в шине велосипеда
Сколько молей газа в велосипедной шине объемом 2.00 × 10 −3 м 3 (2,00 л), давление 7,00 × 10 5 Па (манометрическое давление чуть менее 90,0 фунтов / дюйм 2 ) и при температуре 18,0 ° C?
Стратегия
Определите известные и неизвестные и выберите уравнение для решения неизвестного. В этом случае мы решаем закон идеального газа, PV = nRT , для числа молей n .
Решение
Определите известных:
[латекс] \ begin {array} {lll} P & = & 7.3 \ right)} {\ left (8.31 \ text {J / mol} \ cdot \ text {K} \ right) \ left (291 \ text {K} \ right)} \\\ text {} & = & 0. 579 \ text {mol} \ end {array} \\ [/ latex]
Обсуждение
Наиболее удобный выбор для R в этом случае — 8,31 Дж / моль · К, потому что наши известные количества выражены в единицах СИ. Давление и температура получены из начальных условий в Примере 1, но мы получили бы тот же ответ, если бы использовали окончательные значения.
Закон идеального газа можно рассматривать как еще одно проявление закона сохранения энергии (см. Сохранение энергии).Работа, выполняемая с газом, приводит к увеличению его энергии, увеличению давления и / или температуры или уменьшению объема. Эта повышенная энергия также может рассматриваться как увеличенная внутренняя кинетическая энергия, учитывая атомы и молекулы газа.
Закон идеального газа и энергия
Давайте теперь исследуем роль энергии в поведении газов. Когда вы накачиваете велосипедную шину вручную, вы выполняете работу, многократно прилагая силу на расстоянии. Эта энергия идет на повышение давления воздуха внутри шины и повышение температуры насоса и воздуха.
Закон идеального газа тесно связан с энергией: единицы измерения с обеих сторон — джоули. Правая часть закона идеального газа в PV = NkT равна NkT . Этот термин примерно соответствует количеству поступательной кинетической энергии N атомов или молекул при абсолютной температуре T , как мы формально увидим в «Кинетической теории: атомное и молекулярное объяснение давления и температуры». Левая часть закона идеального газа — это PV , который также имеет единицы измерения в джоулях.Из нашего исследования жидкостей мы знаем, что давление — это один из видов потенциальной энергии на единицу объема, поэтому давление, умноженное на объем, является энергией. Важным моментом является то, что в газе есть энергия, связанная как с его давлением, так и с его объемом. Энергия может быть изменена, когда газ выполняет работу по мере расширения — это мы исследуем в разделе «Методы тепло- и теплопередачи» — аналогично тому, что происходит в бензиновых или паровых двигателях и турбинах.
Стратегия решения проблем: закон об идеальном газе
Шаг 1. Изучите ситуацию, чтобы определить, что это идеальный газ. Большинство газов почти идеальны.
Шаг 2. Составьте список того, какие количества указаны или могут быть выведены из проблемы, как указано (определить известные количества). Преобразуйте известные значения в соответствующие единицы СИ (K для температуры, Па для давления, m 3 для объема, молекул для N и молей для n ).
Шаг 3. Определите, что именно необходимо определить в проблеме (определите неизвестные количества).Письменный список полезен.
Шаг 4. Определите, известно ли количество молекул или количество молей, чтобы решить, какую форму закона идеального газа использовать. Первая форма — PV = NkT и включает N , количество атомов или молекул. Вторая форма — PV = nRT и включает n , количество молей.
Шаг 5. Решите закон идеального газа для количества, которое необходимо определить (неизвестное количество).Вам может потребоваться взять отношение конечных состояний к начальным состояниям, чтобы исключить неизвестные количества, которые остаются фиксированными.
Шаг 6. Подставьте известные величины вместе с их единицами измерения в соответствующее уравнение и получите численные решения с указанием единиц. Обязательно используйте абсолютную температуру и абсолютное давление.
Шаг 7. Проверьте ответ, чтобы узнать, разумен ли он: имеет ли он смысл?
Проверьте свое понимание
Жидкости и твердые вещества имеют плотность примерно в 1000 раз больше, чем газы.Объясните, как это означает, что расстояния между атомами и молекулами в газах примерно в 10 раз больше, чем размер их атомов и молекул.
Решение
Атомы и молекулы в твердых телах и жидкостях расположены близко друг к другу. В газах они разделены пустым пространством. Таким образом, газы имеют меньшую плотность, чем жидкости и твердые тела. Плотность — это масса на единицу объема, а объем связан с размером тела (например, сферы) в кубе. Таким образом, если расстояние между атомами и молекулами увеличивается в 10 раз, то занимаемый объем увеличивается в 1000 раз, а плотность уменьшается в 1000 раз.
Сводка раздела
- Закон идеального газа связывает давление и объем газа с количеством молекул газа и температурой газа.
- Закон идеального газа можно записать через количество молекул газа: PV = NkT , где P — давление, V — объем, T — температура, N — число. молекул, k — постоянная Больцмана k = 1,38 × 10 –23 Дж / K.
- Моль — это количество атомов в образце углерода-12 массой 12 г.
- Число молекул в молье называется числом Авогадро NA , NA = 6,02 × 10 23 моль -1 .
- Моль любого вещества имеет массу в граммах, равную его молекулярной массе, которая может быть определена из периодической таблицы элементов.
- Закон идеального газа также может быть записан и решен в терминах количества молей газа: PV = nRT , где n — количество молей, а R — универсальная газовая постоянная, R = 8 .31 Дж / моль ⋅ К.
- Закон идеального газа обычно действует при температурах, значительно превышающих температуру кипения.
Концептуальные вопросы
Узнайте человеческое население Земли. Есть ли на Земле крот людей? Если средняя масса человека 60 кг, рассчитайте массу родинки людей. Как соотносится масса крота людей с массой Земли?
При каких обстоятельствах вы ожидаете, что газ будет вести себя значительно иначе, чем предсказывает закон идеального газа?
Газовый термометр постоянного объема содержит фиксированное количество газа.Какое свойство газа измеряется, чтобы указать его температуру?
Задачи и упражнения
- Манометрическое давление в шинах вашего автомобиля составляет 2,50 × 10 5 Н / м 2 при температуре 35,0ºC, когда вы едете на пароме на Аляску. Какое у них манометрическое давление позже, когда их температура упадет до –40,0ºC?
- Преобразование абсолютного давления 7,00 × 10 5 Н / м 2 в манометрическое давление в фунтах / дюйм 2 .(Это значение было заявлено чуть меньше 90,0 фунтов / дюйм 2 в Примере 4. Это так?)
- Предположим, что газовая лампа накаливания изготовлена таким образом, что газ внутри лампы находится под атмосферным давлением, когда температура лампы составляет 20,0 ° C. (a) Найдите манометрическое давление внутри такой колбы, когда она горячая, при условии, что ее средняя температура составляет 60,0ºC (приблизительное значение), и пренебрегая любыми изменениями в объеме из-за теплового расширения или утечки газа. (b) Фактическое конечное давление для лампочки будет меньше, чем рассчитано в части (а), потому что стеклянная колба расширится.Каким будет фактическое конечное давление с учетом этого? Это незначительная разница?
- Большие шары, наполненные гелием, используются для подъема научного оборудования на большие высоты. а) Каково давление внутри такого воздушного шара, если он начинается на уровне моря с температурой 10,0 ° C и поднимается на высоту, на которой его объем в двадцать раз превышает первоначальный объем, а его температура составляет –50,0 ° C? б) Какое манометрическое давление? (Предположим, что атмосферное давление постоянно.)
- Подтвердите, что единицами измерения nRT являются единицы энергии для каждого значения R: (a) 8.31 Дж / моль K, (b) 1,99 кал / моль K и (c) 0,0821 л атм / моль ⋅ K.
- В тексте было показано, что N / V = 2,68 × 10 25 м −3 для газа на СТП. (a) Покажите, что это количество эквивалентно N / V = 2,68 × 10 19 см −3 , как указано. (b) Примерно сколько атомов содержится в одном мкм 3 (кубический микрометр) в STP? (c) Что ваш ответ на часть (b) подразумевает разделение атомов и молекул?
- Рассчитайте количество родинок в 2.00-литровый объем воздуха в легких обычного человека. Учтите, что температура воздуха 37,0 ° C (температура тела).
- У пассажира самолета в желудке 100 см. 3 воздуха прямо перед вылетом из аэропорта на уровне моря. Какой объем будет в воздухе на крейсерской высоте, если давление в салоне упадет до 7,50 × 10 4 Н / м 2 ?
- (a) Каков объем (в км 3 ) числа песчинок Авогадро, если каждое зерно представляет собой куб и имеет стороны равные 1.0 мм в длину? (b) Сколько километров протяженностью пляжей это покрыло бы, если бы ширина пляжа в среднем составляла 100 м, а глубина — 10,0 м? Пренебрегайте воздушными промежутками между зернами.
- Дорогая вакуумная система может достичь давления всего 1,00 × 10 –7 Н / м 2 при 20ºC. Сколько атомов в кубическом сантиметре при таком давлении и температуре?
- Плотность атомов газа в определенном месте в космосе над нашей планетой составляет примерно 1,00 × 10 11 м −3 , а давление равно 2.75 × 10 –10 Н / м 2 в этом пространстве. Какая там температура?
- Велосипедная шина имеет давление 7,00 × 10 5 Н / м 2 при температуре 18,0 ° C и содержит 2,00 л газа. Каким будет его давление, если вы выпустите воздух объемом 100 см3 при атмосферном давлении? Предположим, что температура и объем шины остаются постоянными.
- Газовый баллон высокого давления содержит 50,0 л токсичного газа при давлении 1,40 × 10 7 Н / м 2 и температуре 25.0ºC. Его клапан протекает после падения баллона. Цилиндр охлаждается до температуры сухого льда (–78,5 ° C), чтобы снизить скорость утечки и давление, чтобы его можно было безопасно отремонтировать. (а) Каково конечное давление в резервуаре, если предположить, что утечка газа при охлаждении незначительна, и что фазового перехода нет? б) Какое будет конечное давление, если одна десятая часть газа улетучится? (c) До какой температуры необходимо охладить резервуар, чтобы снизить давление до 1,00 атм (при условии, что газ не меняет фазу и что во время охлаждения нет утечки)? (d) Является ли охлаждение резервуара практическим решением?
- Найдите количество родинок в 2.00 л газа при 35,0ºC и давлении 7,41 × 10 7 Н / м 2 давления.
- Вычислите глубину, на которую количество мячей Авогадро для настольного тенниса покроет Землю. Каждый шар имеет диаметр 3,75 см. Предположим, что пространство между шарами добавляет дополнительные 25,0% к их объему, и предположим, что они не раздавлены собственным весом.
- (a) Каково манометрическое давление в автомобильной шине 25,0 ° C, содержащей 3,60 моль газа в объеме 30,0 л? (b) Каким будет его манометрическое давление, если вы добавите 1.00 л газа первоначально при атмосферном давлении и 25,0ºC? Предположим, что температура возвращается к 25,0 ° C, а объем остается постоянным.
- (a) В глубоком космосе между галактиками плотность атомов всего лишь 10 6 атомов / м 3 , а температура — холодная 2,7 К. Что такое давление? б) Какой объем (в м 3 ) занимает 1 моль газа? (c) Если этот объем является кубом, какова длина его сторон в километрах?
Глоссарий
закон идеального газа: физический закон, который связывает давление и объем газа с числом молекул газа или числом молей газа и температурой газа
постоянная Больцмана: k , физическая постоянная, которая связывает энергию с температурой; к = 1.38 × 10 –23 Дж / К
Номер Авогадро: NA , количество молекул или атомов в одном моль вещества; NA = 6,02 × 10 23 частиц / моль
моль: количество вещества, масса которого (в граммах) равна его молекулярной массе
Избранные решения проблем и упражнения
1. {2} \ right) \\ & = & \ text {N} \ cdot \ text {m} = \ text {J} \ конец {массив} \\ [/ латекс]
7.7,86 × 10 −2 моль
9. (а) 6.02 × 10 5 км 3 ; (б) 6.02 × 10 8 км
11. -73.9ºC
13. а) 9,14 × 10 6 Н / м 2 ; (б) 8,23 × 10 6 Н / м 2 ; (в) 2,16 К; (d) Нет. Требуемая конечная температура слишком низкая, чтобы ее можно было легко достичь для большого объекта.
15. 41 км
17. (а) 3,7 × 10 −17 Па; (б) 6.0 × 10 17 м 3 ; (в) 8.4 × 10 2 км
Аренда резервуара с гелием| Liberty Industrial Gases and Welding Supply, Inc.
(Liberty Industrial Gases поставляет полный спектр промышленных газов в баллонах различных размеров для всех ваших потребностей в газе. Возможность подачи чистых газов вместе с индивидуальным смешиванием компонентов газов для удовлетворения всех ваших сварочных потребностей.)
Свойства гелия
Гелий — безвкусный, негорючий, нетоксичный, инертный газ без запаха.Самая маленькая из всех молекул, гелий — второй по лёгкости элементарный газ после водорода.
Гелий постоянно образуется в результате радиоактивного распада урана и других элементов, постепенно проникая в атмосферу. Однако коммерческое извлечение из воздуха нецелесообразно, поскольку концентрация гелия составляет всего около пяти частей на миллиард.
Большая часть мирового гелия поступает из Техаса, Оклахомы, Канзаса и восточного склона Скалистых гор, другие источники включают Ближний Восток и Россию.Praxair производит гелий на своих предприятиях в Буштоне и Улиссе, штат Канзас, и предлагает возможности для распространения по всему миру
Гелий — инертный газ без цвета, запаха и вкуса, не обладающий токсичными свойствами. Член химического семейства инертных газов, он на 1/7 тяжелее воздуха. Жидкий гелий при -452ºF — самый холодный сжиженный газ.
Спецификация G-9.1-1992 ассоциации сжатого газа (CGA), тип I, класс D считается промышленным стандартом газообразного гелия.
(единицы в ppm (об. / Об.), Если не указано иное)
| Предельные характеристики | CGA G-9.1 Тип I, марка D | Типичный |
| Гелий минимум,% | 99,5 | 99,7 |
| Максимально гарантированное количество примесей | – | 50 |
| Вода | 15 | 15 |
| Точка росы, ° F | – | – |
| Кислород | 5 | 5 |
| Азот | – | – |
Жидкий гелий типа II при пропускании через 10-микронный абсолютный фильтр при давлении менее 5.2ºK — это чистый гелий, анализ которого не требуется.
Содержание воды в гелии, необходимое для любого конкретного сорта и применения, может варьироваться в зависимости от предполагаемого использования. Если требуется конкретный предел, его следует указать как предельную концентрацию, выраженную в ppm (об. / Об.) Или эквиваленте точки росы. Также обратите внимание, что содержание воды марок 4,5 и выше будет примерно на 10 частей на миллион выше при поставке в стеклянных колбах из пирекса.
Уровни проверки качества применимы только к газообразному гелию.Пределы примесей для жидкого гелия не указаны, поскольку отсутствуют достаточные технические данные и аналитические процедуры, чтобы гарантировать окончательную количественную спецификацию. Требование гарантировать, что загруженная текучая среда в контейнере представляет собой жидкий гелий, может быть удовлетворено путем анализа отходящего газа транспортного контейнера или демонстрации того, что температура загруженной текучей среды ниже тройной точки водорода (13,88К).
Данные преобразования гелия
| Гелий | Масса | Газ | Жидкость | |||
| фунтов | Килограмм | Кубических футов | Кубических метров | галлонов | литров | |
| фунтов | кг | SCF | См3 | Гал | л | |
| 1 фунт | 1 | 0.4536 | 96,71 | 2,736 | 0,9593 | 3,631 |
| 1 килограмм | 2,205 | 1 | 213,2 | 6.039 | 2,115 | 8.006 |
| 1 SCF газа | 0,0103 | 0.00469 | 1 | 0,02832 | 0,009919 | 0,03754 |
| 1 Sm3 Gas | 0,3651 | 0,1656 | 35,31 | 1 | 0,3504 | 1,3257 |
| 1 галлон жидкости | 1.0423 | 0.4728 | 100,8 | 2,854 | 1 | 3,785 |
| 1 л Жидкость | 0,2754 | 0,1249 | 26,63 | 0,7542 | 0,2642 | 1 |
SCF (стандартный кубический фут) и SM3 (стандартный кубический метр) газа, измеренные при 1 атмосфере и температуре 70 ° F.
Жидкость измерена при 0ºF и давлении насыщения.
Нм3 (нормальный кубический метр) газа при 1 атмосфере и 0ºC.
Все значения округляются до ближайших 4/5 значащих чисел.
Самый лучший блог о воздушных шарах: гелий
В первой части этого блога, состоящего из двух частей, мы рассмотрели гелий и кое-что из того, что вам нужно знать как профессионалу в области воздушных шаров, а также краткое введение в расчет затрат.Тем не менее, для тех из вас, кто действительно хочет понять, как рассчитать свои затраты на гелий для всех размеров воздушных шаров, продолжайте читать, я надеюсь, что мне удалось это хорошо объяснить? Гелиевые баллоны различаются в зависимости от их размера и давления (бар или фунт / кв. Дюйм), до которого они наполняются, поэтому очень важно знать, что вы используете, без этой информации вы не сможете рассчитать свои затраты.
Мир разделен метрическими и имперскими расчетами, что сделало этот блог немного более сложным для написания, поэтому я решил показать оба, начиная с метрической системы, прокрутите вниз для имперских расчетов.
METRIC Расчеты:
В приведенной выше таблице показаны 3 размера баллона с указанием кода размера каждого баллона, объема / кубических метров = м3) и бар давления, а также другая информация, такая как вес, высота и диаметр баллона.
| Датчик, показывающий только показания стержней |
Цилиндр размером L = 9 м3 (317 куб. Футов)
Цилиндр размером T = 3,60 м3 (127 куб. Футов)
Цилиндр размером V = 1,81 м3 (63 куб.фут)
Математика никогда не была моей сильной стороной, поэтому я надеюсь, что смогу объяснить это, чтобы вы поняли.
Чтобы определить, сколько гелия содержится в вашем баллоне, вам необходимо произвести следующий расчет.
Во-первых, нам нужно знать объем нашего цилиндра в литрах, чего нет в приведенной выше таблице. Чтобы узнать это, мы берем объем, который для цилиндра размера L составляет 9 м3 x 1000 = 9000, теперь разделим его на показание давления в барах, равное 200, что дает нам 45 литров.
Умножьте объем в литрах на давление в баллоне (это давление в барах, указанное на вашем регуляторе), а затем разделите на 1000, чтобы получить объем в кубических метрах.
Итак, допустим, что у нас есть неиспользованный 45-литровый баллон (размер L), который показывает 200 бар (полный)
45 (объем в литрах) x 200 (давление бар) = 9000 ÷ 1000 = 9 м3 гелия в баллоне, что мы уже знаем.
Теперь, что, если бы мы уже использовали часть гелия и показания в столбике говорят, что у нас давление только 50 бар, сумма будет выглядеть так:
45 (объем в литрах) x 50 (давление в барах) = 2250 ÷ 1000 = 2,25 м3 гелия, остающегося в баллоне.
Итак, как мы можем использовать эту информацию, чтобы сказать нам, сколько воздушных шаров мы можем надуть из этого цилиндра.
Qualatex предоставила нам всю информацию, которая нам нужна для этого, они создали 2 диаграммы, одну для латексных и хлоропреновых баллонов, а другую — для баллонов Microfoil®. Существует отличная загружаемая диаграмма гелия, просто нажмите здесь и храните ее в удобном для поиска месте на вашем компьютере, чтобы вы могли легко рассчитать свои затраты на гелий.
| Это образец загружаемой гелиевой диаграммы, но, поскольку она занимает 5 страниц, я только что показал вам несколько первых строк! |
Итак, глядя на таблицу под заголовком «Емкость газа», я вижу, что для 11-дюймовых латексных воздушных шаров, надутых до 11 дюймов, требуется 0,5 куб. Фута (кубический фут) или 0,015 м3 кубического метра гелия.
Поскольку мы работаем в метрических единицах, а не в британских, нам нужна вторая цифра (кубические метры), указанная в скобках на диаграмме, чтобы рассчитать, сколько 11-дюймовых воздушных шаров мы можем надуть из нашего цилиндра.
Это был наш первый расчет
45 (объем в литрах) x 200 (давление бар) = 9000 ÷ 1000 = 9 м3 гелия в баллоне.
Итак, если мы знаем, что у нас в цилиндре 9 м3 гелия, мы можем разделить 9 на 0,015 = 600, поэтому в нашем цилиндре достаточно гелия, чтобы надуть 600 11-дюймовых латексных воздушных шаров.
Теперь для нашего второго расчета:
Теперь, что, если бы мы уже использовали часть гелия, а показание столбика говорит, что у нас осталось только 50 бар, сумма будет выглядеть так:
45 (емкость в литрах) x 50 (давление бар) = 2500 ÷ 1000 = 2,25 м3 гелия, остающегося в баллоне.
Итак, мы знаем, что в нашем цилиндре осталось 2,25 м3, и мы можем разделить 2,25 на 0,015 = 150 — следовательно, в нашем цилиндре достаточно гелия, чтобы надуть 150 11-дюймовых латексных воздушных шаров.
Посмотрим, сможете ли вы выяснить, сколько гелия осталось в этих баллонах и сколько 11-дюймовых воздушных шаров мы можем надуть из оставшегося газа?
| Манометр 1 |
18 x 185 (бар) = 3330 разделить на 1000 = 3,33 м3 гелия, оставшегося в цилиндре 3,33 разделенного на 0,015 = 222 — следовательно, в нашем цилиндре все еще достаточно гелия, чтобы надуть 222 11-дюймовых латексных шара.
| Калибр 2 |
Манометр 2. Показывает манометр, который показывает, что в баллоне осталось всего 30 бар. Опять же, это цилиндр размера T, который при заполнении содержит 3 бара.Объем 6м3, что эквивалентно 18 литрам.
18 x 30 = 540, разделить на 1000 = 0,54, разделить на 0,015 = 36 — поэтому в цилиндре у нас достаточно гелия, чтобы надуть 36 11-дюймовых латексных шаров.
Теперь давайте воспользуемся теми же показаниями, но на этот раз посмотрим, сколько 16-дюймовых гео-пончиков мы можем надуть из оставшегося гелия?
Во-первых, нам нужно знать, каков объем газа для 16-дюймового гео-пончика, и, глядя на график, он говорит мне, что он составляет 0,7 куб. Фута или (.020м3).
Итак, для калибра 1 мы уже знаем, что в нашем цилиндре 3,33 м3 гелия. Итак, на этот раз мы разделим 3,33 на 0,020 = 166 — значит, у нас достаточно гелия, чтобы надуть гео-пончики размером 166 x 16 дюймов.
Калибр 2, в нашем баллоне всего 0,54 м3 гелия, 0,54 деленное на 0,020 = 27 — следовательно, в этом баллоне остается только гелий, достаточный для надувания воздушных шаров Geo Donut 27 x 16 дюймов.
Теперь мы понимаем, как рассчитать, сколько воздушных шаров вы можете надуть из любого баллона…
Итак, давайте посмотрим, сколько воздушных шаров мы сможем выпустить из цилиндра объемом 3,6 м3.
Мы можем рассчитать это сами, используя уже имеющуюся информацию:
3,6 (объем), разделенные на использование газа каждым воздушным шаром, скажут нам, сколько воздушных шаров мы можем получить из баллона такого размера.
3,6 ÷ 0,0141 = 255–11 дюймов латекс
3,6 ÷ 0,2266 = 15–30 дюймов латекс
3,6 ÷ 0,037 = 97–35 дюймов полумесяца
IMPERIAL Calculations
На этот раз мы работаем с кубическими метрами цилиндра, а не с кубическими метрами.
Итак, давайте посмотрим на преобразование между барным давлением и давлением в фунтах на квадратный дюйм.
1 бар = 14,50 фунтов на квадратный дюйм или фунт / кв. Дюйм
, следовательно, 200 бар = 2900 фунтов на кв. Дюйм
| Манометр, который показывает показания как в фунтах на квадратный дюйм, так и в барах |
Я поискал в Интернете и увидел, что гелиевые цилиндры бывают разных размеров в США, и не могу найти диаграмму цилиндров, подобную той, которую я использовал в метрическом примере, поэтому мы будем использовать некоторые примеры размеров цилиндров, которые я нашел.
Резервуар 280 куб. Футов
Резервуар 242 куб. Футов
Резервуар 137 куб. Футов
Резервуар 110 куб. Футов
Резервуар 55 куб. Футов
Я не совсем уверен, какой размер чаще всего используют художники по воздушным шарам в США?
Итак, давайте начнем с резервуара на 280 куб. Футов, который при заполнении показывает 2200 фунтов на квадратный дюйм на манометре, на этот раз это внешние числа.
Так что это довольно простой процесс. Глядя на диаграмму использования газа, мы видим, что 11-дюймовому баллону требуется 0,5 куб. Фута газа, чтобы надуть его до 11 дюймов.
280 (объем в кубических футах) разделить на 0,5 = 560 — следовательно, мы знаем, что из этого цилиндра можно ожидать надувания 560 11-дюймовых воздушных шаров.
Если бы вы использовали бак емкостью 137 куб. Футов, математика выглядела бы так:
137 разделить на 0,50 = 274, поэтому из цилиндра этого размера мы ожидаем надуть воздушный шар 274 11 дюймов. S
Теперь, чтобы определить, сколько воздушных шаров вы можете надуть из частично использованного баллона, вам необходимо знать, какое было давление в фунтах на квадратный дюйм, когда баллон был доставлен вам.
В Великобритании баллоны заполняются при 200 бар, 200 бар = 2900, однако, насколько я понимаю в США и других странах, они не заполняются до такого высокого давления, поэтому вам нужно будет проверить, для этого примера мы будем использовать 2200 фунтов на кв. Дюйм.
Итак, первое, что нам нужно рассчитать, — это давление в фунтах на квадратный дюйм на 11-дюймовый баллон.
2200 разделить на 560 = 3,93 фунта на квадратный дюйм на 11-дюймовый баллон.
Итак, проверьте, что показывает ваш цилиндр, например, 1500 фунтов на квадратный дюйм:
1500 делится на 3.93 = 381 — следовательно, он говорит нам, что в нашем цилиндре достаточно гелия, чтобы надуть 381 11-дюймовый воздушный шар.
Давайте сделаем то же самое снова, но на этот раз с воздушным шариком другого размера, скажем, с воздушными шариками диаметром 16 дюймов.
Во-первых, нам нужно знать, сколько гелия вмещает воздушный шар диаметром 16 дюймов, что, глядя на диаграмму, показывает мне 1,5 кубических фута (в 3 раза больше, чем воздушный шар диаметром 11 дюймов).
Итак, если мы используем резервуар на 280 куб. Футов, мы разделили 280 на 1,5 = 186 — таким образом, мы можем надуть 186 16-дюймовых воздушных шаров из резервуара объемом 280 куб. Футов.
Теперь нам нужно рассчитать давление в фунтах на квадратный дюйм на воздушный шар диаметром 16 дюймов.
2200 разделить на 186 = 11,82 фунтов на квадратный дюйм на воздушный шар диаметром 16 дюймов
Если в нашем цилиндре осталось 1500 фунтов на квадратный дюйм, мы разделим 1500 на 11,82 = 126 — в нашем цилиндре осталось достаточно гелия, чтобы надуть 126 воздушных шаров диаметром 16 дюймов.
Вот еще кое-что, что нам нужно учитывать:
Показания PSI могут отличаться, когда цилиндр заполнен, поэтому они не всегда могут быть одинаковыми в одно и то же время. Также имейте в виду, что температура влияет на давление (более высокая температура = более высокое давление, более низкая температура = более низкое давление
Если у вас есть диаграмма использования гелия (на которую я создал ссылку в этом блоге или вы можете найти ее в каталогах Qualatex Everyday) и вы знаете, сколько требуется каждому размеру и типу воздушного шара, чтобы надуть до нужного размера и размер баллона, с которым вы работаете, вы должны иметь возможность вычислить, сколько воздушных шаров каждого размера вы можете надуть из своего баллона, и если вы знаете, сколько вам стоит ваш гелий из расчета на один баллон, вы можете рассчитать, сколько Стоимость гелия также указана за баллон.
Пожалуйста, помните, что если вы не используете прецизионное оборудование для накачивания, такое как Duplicator 2 или Dual Split Second Sizer, который точно измеряет гелий при нажатии ножной педали (в зависимости от настройки времени v давления), эти расчеты могут быть только приблизительными, как Все представления о 11-дюймовом воздушном шаре немного отличаются, и некоторые люди выпускают небольшое количество гелия при использовании калибровочных коробок / шаблонов, что приводит к потере гелия и сокращает количество воздушных шаров, которые вы сможете надуть из своего баллона.
Я надеюсь, что эта информация поможет некоторым из вас?
Счастливого полета на воздушном шаре!
Сью
www.suebowler.com
.



